免疫衰老(专业版)
进入老年期免疫功能不断下降,越来越容易受到各种感染或对疫苗反应差,这大多与免疫衰老有关。
英文名称:Immune Senescence
1.先天性免疫(或固有免疫):它是人体对外来和潜在有害物质的第一反应系统,免疫反应迅速,可以非特异性地攻击引发免疫反应的抗原物。其关键组成部分包括如下:
2.适应性免疫(或获得性免疫):在出生后人体逐步建立起来,通过针对特定外来抗原产生抗体而发挥免疫作用。如果先天免御系统没有消除威胁,那么下一级防御就是适应性免疫,其对个体抗原做出特异性反应。获得性免疫具有记忆能力,如注射麻疹疫苗后,就不会再发生麻疹感染。适应性免疫包括抗体和细胞介导的免疫:
有助于防控免疫衰老的营养和草本补充剂,主要包括如下:
1.锌:
锌是一种重要的微量矿物质,对健康的免疫功能至关重要。锌缺乏在老年人中很常见,并导致免疫功能的变化,类似于免疫衰老1,2。与缺锌相关的免疫改变包括胸腺功能下降、对疫苗的抗体反应降低以及吞噬细胞和NK细胞功能受损2,3。
在一项针对健康老年志愿者的研究中,与安慰剂相比,一年内每天摄入45mg锌可使感染发生率降低67%。服用锌的患者的肿瘤坏死因子α(一种炎症细胞因子)水平也大大降低4。在一项针对养老院老年人的研究中,与缺锌的人相比,锌水平正常的居民肺炎的发病率明显较低。锌充足的个体肺炎持续时间更短,抗生素使用率降低50%,全因死亡率更低5。一项针对老年人的对照临床试验显示,在六个月内每天补充45mg锌可降低血浆炎症标志物,包括IL-6和C反应蛋白6。
将锌与其他重要的维生素和矿物质结合也可能有助于免疫功能。在一项随机对照试验中,招募了42名年龄在55岁至75岁之间的受试者,与服用安慰剂的人相比,服用含有10mg锌和1000mg维生素C以及其他维生素和矿物质的复合维生素/矿物质补充剂12周的人自报患病天数更少,症状也不那么严重。使用补充剂后,病假天数减少了近65%7。
2.维生素E:
充足的维生素E对维持有效的免疫功能至关重要。事实上,各种动物研究表明,维生素E缺乏会引发免疫抑制。临床证据表明,补充维生素E可以增加对感染的抵抗力,尤其是在老年人中8,9。
在一项针对老年男性和女性的研究中,每天补充200mg维生素E可显著增强免疫参数,包括中性粒细胞、T细胞、B细胞和NK细胞功能,使其值接近年轻健康成年人10。
增加维生素E的摄入量已被证明可以恢复与衰老相关的T细胞功能的下降。这种T细胞功能的改善源于维生素E对T细胞的直接影响以及对前列腺素E2的抑制,前列腺素E2是炎症介质和T细胞抑制剂9,11。在小鼠模型中,补充维生素E逆转了与年龄相关的幼稚T细胞功能下降12。
3. N-乙酰半胱氨酸:
NAC是含硫氨基酸半胱氨酸的一种形式,它是谷胱甘肽的前体,谷胱甘肽是代谢解毒的重要促进剂13-15。谷胱甘肽在调节炎症反应中起着关键作用,尤其是在肺部。它对某些免疫功能至关重要,包括T细胞的增殖以及中性粒细胞和树突状细胞的细胞杀伤活性。谷胱甘肽细胞水平的降低与感染易感性的增加有关16。
在一项针对262名流感和流感样疾病高危人群的对照临床试验中,六个月内每天两次600mg的NAC补充剂显著降低了流感和流感症状的频率和严重程度,如咳嗽、喉咙痛、头痛以及肌肉和关节疼痛。NAC预防流感症状的能力在冬季尤为明显。在研究期间流感病毒感染检测呈阳性的人中,NAC组只有25%出现症状性疾病,而安慰剂组为79%17。透析患者在八周内使用相同的NAC剂量,导致炎症标志物水平显著降低,包括C反应蛋白、肿瘤坏死因子α和IL-618。
4.维生素C:
维生素C支持先天免疫系统和适应性免疫系统的功能,在防御细菌和病毒方面发挥着重要作用。除了刺激免疫力外,维生素C似乎还可以抑制过度的免疫活性,可能部分是通过干扰炎症细胞因子的合成19-21。
新增加的证据表明,随着年龄的增长,补充维生素C可能有助于维持免疫功能。在维生素C缺乏和过早衰老的小鼠模型中,补充较高剂量的维生素C(相当于79.5kg体重的人每天大约1300mg)与较低剂量(相当于79.5kg体重的人每天约130mg)进行了比较。一年后,接受高剂量维生素C的小鼠比接受低剂量维生素C小鼠表现出更好的胸腺保存和更大的免疫细胞计数22。
一项对安慰剂对照试验的大型分析结果表明,补充维生素C可以缩短感冒的持续时间,成人和儿童分别减少8%和14%。此外,该分析发现,维生素C补充剂将马拉松运动员等剧烈体力消耗人群的感冒发病率降低了一半23。
5.乳铁蛋白:
乳铁蛋白是一种铁结合蛋白,存在于身体分泌物中,包括母乳、唾液、眼泪、鼻腔分泌物、肠液以及中性粒细胞中。乳铁蛋白的抗菌作用包括破坏微生物细胞膜,结合和分离铁,而铁是几乎所有细菌生长和繁殖所需的24,25。无铁形式的乳铁蛋白(脱乳铁蛋白)是一种有效的铁结合蛋白,并已被证明具有抗菌作用24,26,27。
乳铁蛋白对包括细菌、病毒、真菌和寄生虫在内的多种微生物具有直接的抗菌活性25,28,29。在一项动物研究中,69%的经静脉注射乳铁蛋白预处理的小鼠在给予致命剂量的有毒大肠杆菌后存活了30天,而只有4%的对照小鼠存活30。
6.乳清蛋白:
乳清是奶酪制作过程中从凝乳中分离出来的液体。源自乳清的产品已证明具有免疫调节特性31,32。乳清蛋白特别富含参与谷胱甘肽合成的前体氨基酸,谷胱甘肽是一种具有抗炎特性的强大自由基清除剂。谷胱甘肽对先天免疫和适应性免疫都至关重要31,33,34。
一项初步研究比较了乳清蛋白和大豆蛋白对17名健康老年人疫苗反应性的影响35。参与者被随机分配在四周内食用乳清蛋白或大豆蛋白。然后,他们接种了肺炎球菌疫苗,并在接种后继续补充蛋白质四周。与接受大豆蛋白的人相比,接受乳清蛋白的人对14种肺炎球菌中的12种表现出更强的抗体反应,其中包括四种最有害的细菌。研究人员得出结论,“补充乳清蛋白是一种很有前途的补充剂,可以刺激老年人对疫苗的免疫反应,并可能抵消(免疫衰老),同时需要进行更大规模的研究。”
在另一项针对12名健康志愿者的临床试验中,单剂量乳清提取物是比安慰剂更有效的免疫激活剂,可以快速提高某些免疫细胞的微生物吞噬活性,并动员新的NK细胞进入循环36。在一项对培养的中性粒细胞的研究中,乳清蛋白提取物没有立竿见影的效果,而是具有启动作用,24小时后提高了中性粒细胞活性32。
7.灵芝:
灵芝是一种药用蘑菇,在亚洲用于免疫系统支持已有2000多年的历史。灵芝含有多糖、三萜和其他潜在的活性化合物。实验室和动物研究表明,灵芝多糖具有免疫调节、抗肿瘤和细胞杀伤作用,这似乎部分源于其影响T细胞、NK细胞和巨噬细胞的能力37-39。
灵芝多糖中的β-葡聚糖已被发现可刺激先天免疫反应和适应性免疫反应38。其他灵芝化合物已证明具有抗病毒特性,包括对单纯疱疹病毒、乙肝病毒和EB病毒的活性。灵芝成分也已被证明能抑制酵母和大肠杆菌的生长40-43。
这些免疫增强作用可能有助于解释一项动物研究的结果,在该研究中,补充灵芝的小鼠比对照小鼠活得更长44。在另一项研究中,含有绿茶提取物和富含多糖和三萜的灵芝提取物的产品刺激免疫细胞的增殖,包括B细胞、T细胞和NK细胞,并抑制小鼠的恶性肿瘤45。
一项对临床对照试验的严格审查发现,癌症患者在化疗和放疗的同时使用灵芝,比未使用灵芝的患者对癌症治疗的积极反应高50%。灵芝还增加了T细胞的几个亚群的百分比,并且可能略微增加了NK细胞的活性。作者得出的结论是,灵芝可以被认为是“考虑到其增强肿瘤反应和刺激宿主免疫的潜力,作为传统治疗的替代辅助手段”38。
8.脱氢表雄酮(DHEA):
DHEA是一种在健康免疫系统功能中发挥主要作用的类固醇激素46,47。DHEA水平随着年龄的增长而显著下降。到80岁时,DHEA水平降至峰值的10-20%48,49。
一项针对平均年龄63岁、血清DHEA-S水平较低的男性的临床试验发现,口服补充DHEA可以迅速纠正DHEA状态。与安慰剂相比,DHEA治疗改善了免疫参数,包括单核细胞水平、B-和T-细胞功能以及NK细胞水平50。在一项针对38名参与者的小型观察性研究中,唾液DHEA水平与唾液杀菌活性呈正相关,后者是衡量先天免疫功能的指标51。另一项观察性研究指出,低水平的DHEA和高水平的IL-6之间存在关联,而IL-6是一种与免疫衰老有关的炎症细胞因子。此外,DHEA还能抑制来自研究参与者的免疫细胞产生IL-652,53。根据一项针对老年小鼠的研究,DHEA也可能增强对流感疫苗的免疫反应54。
DHEA作为皮质醇的平衡物发挥着关键作用。皮质醇是一种具有免疫抑制特性的肾上腺激素,而DHEA可能具有直接的免疫刺激特性:在一项对65岁以上捐献者白细胞的实验室研究中,DHEA治疗逆转了免疫细胞上特异性受体与年龄相关的减少,并提高了免疫细胞的反应性55。尽管DHEA水平随着年龄的增长而急剧下降,但皮质醇水平保持相对恒定,导致这两种激素失衡,这被认为有助于免疫衰老46,56。
10.β-葡聚糖:
β-葡聚糖是一种多糖(碳水化合物),存在于细菌、真菌、谷物(包括燕麦)和藻类的细胞壁中。β-葡聚糖是对灵芝等药用蘑菇的免疫调节益处负责的活性成分之一57-59。
已发现β-葡聚糖可调节免疫活性的多个方面,具有显著的抗肿瘤和抗菌特性60-62。2013年的一项研究综述发现,含有β-葡聚糖的植物提取物提高了癌症患者的存活率和生活质量。这篇综述还发现,β-葡聚糖提取物减少了几种不同形式癌症化疗和放疗的副作用59。
肿瘤细胞通过抑制免疫功能和诱导免疫耐受的机制逃避免疫系统63。一项研究表明,β-葡聚糖可能通过降低受肿瘤信号影响的调节性免疫细胞的抑制功能,帮助克服癌症细胞消除的障碍64。
一些富含β-葡聚糖的药用蘑菇包括:蘑菇菌丝体专利品牌AHCC®,云芝蘑菇等。
9.酶改性米糠:
经酶修饰的米糠是米糠的衍生物,已被证明可以增强免疫细胞,特别是NK细胞的数量和功能65-67。这种经过特殊修饰的米糠是增强免疫的阿拉伯木聚糖的来源68,该多糖已被证明可以预防70至95岁人群的上呼吸道病毒感染69。酶改性米糠的多糖部分也表现出抗菌和抗癌特性70。事实上,几位研究人员提出,酶改性米糠作为癌症的辅助治疗可能是有益的65,71,72。
一系列实验室和动物实验表明,酶改性的米糠提高了几种免疫细胞的活性,包括中性粒细胞、单核细胞、巨噬细胞和树突状细胞73-76。在2013年一项针对多发性骨髓瘤患者的研究中,补充酶改性米糠产品可提高NK细胞活性66。酶改性米糠还使培养的乳腺癌症细胞对化疗药物的易感性增加了100倍以上71。
11.穿心莲:
穿心莲是一种亚洲传统的草药,用于治疗感染、感冒、发烧和炎症。在2010年对荷瘤小鼠的一项研究中,穿心莲及其活性成分之一穿心莲内酯增强了NK细胞和其他免疫细胞破坏癌症细胞的能力77,78。
疫苗有效性降低是免疫衰老的一个突出特征79-81,有证据表明穿心莲可能改善对疫苗的免疫反应。在一项针对小鼠的研究中,口服穿心莲提取物和穿心莲内酯都能增强抗体的产生,并激活免疫细胞以应对沙门氏菌疫苗82。
12.大蒜:
大蒜以其改善心血管危险因素的能力而闻名,它还具有免疫调节和免疫刺激特性,以及抗肿瘤作用83-85。
对已发表的临床试验数据的详细审查发现,大蒜补充剂可以显著减少上呼吸道感染的数量、持续时间和严重程度。这篇综述还发现,大蒜补充剂通过增加巨噬细胞活性、NK细胞数量以及T和B细胞的产生来刺激免疫功能86。在一项临床试验中,120名21-50岁的健康参与者被分配在感冒和流感季节每天使用2.56g陈蒜提取物或安慰剂,持续90天。补充大蒜与降低感冒和流感的严重程度以及增加细胞毒性T细胞和NK细胞的增殖和活性有关87。在动物研究中,大蒜已被证明可以增加抗体的产生,并增强巨噬细胞、细胞毒性T细胞和NK细胞的细胞杀伤活性88。其他动物研究表明,老化的大蒜提取物可以防止与心理压力相关的免疫抑制89。
有趣的是,大蒜也被证明可以抑制与过敏反应相关的过度活跃的免疫反应。来自实验研究的数据表明,陈化大蒜提取物可以减少组胺的释放,并改变参与过敏反应的免疫细胞的功能85。
13.岩藻聚糖:
某些日本人的预期寿命是世界上最长的。经常食用富含岩藻聚糖(Fucoidan,又称褐藻糖胶)的棕色海藻可能有助于他们的长寿。研究表明,褐藻糖胶具有增强免疫、抗炎、抗病毒和抗肿瘤的特性90-92。
2014年一项实验室和动物研究的证据表明,褐藻糖胶可能诱导抗肿瘤免疫活性,并提高实验性抗肿瘤疫苗的有效性。根据他们的发现,研究作者认为褐藻糖胶可能在未来作为抗癌疫苗的一种成分是有用的90。
在一项针对日本老年志愿者的研究中,发现补充褐藻糖胶可以增加对季节性流感疫苗的免疫反应。与安慰剂组相比,服用褐藻糖胶的志愿者在接种流感疫苗五周后,流感病毒特异性抗体水平更高,NK细胞活性增加。这些发现表明,褐藻糖胶可以通过提高疫苗的有效性来降低免疫功能较差的老年人的感染率并预防严重的健康问题91。
14.青牛胆:
青牛胆(Tinospora cordifolia)是一种用于传统阿育吠陀医学的草药,一直是许多科学研究的主题。从青牛胆中分离出了几种增强免疫功能的化学成分93-95。
从青牛胆中提取的多糖特别令人感兴趣。其中一种复合碳水化合物—阿拉伯半乳聚糖,已被证明可以增强树突细胞的成熟和这些细胞杀死癌症细胞的能力。另一种青牛胆多聚糖(α-葡聚糖),显示出激活NK细胞、B细胞和T细胞的能力,导致其肿瘤细胞杀伤功能的剂量依赖性增加96,97。
动物和临床研究已经证明了青牛胆在一系列条件下具有强大的免疫作用。在一项针对免疫功能受抑制的外科患者的随机临床试验中,一半患者单独接受常规护理,一半患者接受常规护理加上青牛胆补剂。青牛胆组的中性粒细胞功能正常化,但在对照组没有。败血症是一种血液感染和手术的严重并发症,在50%的对照组中很明显,但在接受青牛胆治疗的患者中没有一例98。在大鼠中,青牛胆降低了关节炎炎症、骨和软骨损伤,还降低了炎性细胞因子的水平,包括肿瘤坏死因子α和IL-699。
更多可查看其个性化综合干预方案如下:
以及参阅本网如下专文的有关内容:
参考文献:
1. Cabrera AJ. Zinc, aging, and immunosenescence: an overview. Pathobiol Aging Age Relat Dis. 2015;5:25592.
2. Maywald M et al. Zinc homeostasis and immunosenescence. J Trace Elem Med Biol. Jan 2015;29:24-30.
3. Haase H et al. The immune system and the impact of zinc during aging. Immunity & ageing: I & A. 2009;6:9.
4. Prasad AS et al. Zinc supplementation decreases incidence of infections in the elderly: effect of zinc on generation of cytokines and oxidative stress. The American journal of clinical nutrition. Mar 2007;85(3):837-844.
5. Meydani SN et al. Serum zinc and pneumonia in nursing home elderly. The American journal of clinical nutrition. Oct 2007;86(4):1167-1173.
6. Bao B et al. Zinc decreases C-reactive protein, lipid peroxidation, and inflammatory cytokines in elderly subjects: a potential implication of zinc as an atheroprotective agent. The American journal of clinical nutrition. Jun 2010;91(6):1634-1641.
7. Fantacone ML et al. The Effect of a Multivitamin and Mineral Supplement on Immune Function in Healthy Older Adults: A Double-Blind, Randomized, Controlled Trial. Nutrients. 2020;12(8).
8. Wu D et al. Age-associated changes in immune function: impact of vitamin E intervention and the underlying mechanisms. Endocrine, metabolic & immune disorders drug targets. 2014;14(4):283-289.
9. Han SN et al. Impact of vitamin E on immune function and its clinical implications. Expert review of clinical immunology. Jul 2006;2(4):561-567.
10. De la Fuente M et al. Vitamin E ingestion improves several immune functions in elderly men and women. Free radical research. Mar 2008;42(3):272-280.
11. Wu D et al. Age-associated changes in immune and inflammatory responses: impact of vitamin E intervention. J Leukoc Biol. Oct 2008;84(4):900-914.
12. Adolfsson O et al. Vitamin E-enhanced IL-2 production in old mice: naive but not memory T cells show increased cell division cycling and IL-2-producing capacity. Journal of immunology (Baltimore, Md.: 1950). Oct 1 2001;167(7):3809-3817.
13. Brosnan JT et al. The sulfur-containing amino acids: an overview. The Journal of nutrition. Jun 2006;136(6 Suppl):1636s-1640s.
14. Santus P et al. Oxidative stress and respiratory system: pharmacological and clinical reappraisal of N-acetylcysteine. COPD. Dec 2014;11(6):705-717.
15. Millea PJ. N-acetylcysteine: multiple clinical applications. American family physician. Aug 1 2009;80(3):265-269.
16. Ghezzi P. Role of glutathione in immunity and inflammation in the lung. International journal of general medicine. 2011;4:105-113.
17. De Flora S et al. Attenuation of influenza-like symptomatology and improvement of cell-mediated immunity with long-term N-acetylcysteine treatment. The European respiratory journal. Jul 1997;10(7):1535-1541.
18. Purwanto B et al. Effect of oral N-acetylcysteine treatment on immune system in continuous ambulatory peritoneal dialysis patients. Acta medica Indonesiana. Apr 2012;44(2):140-144.
19. Sorice A et al. Ascorbic acid: its role in immune system and chronic inflammation diseases. Mini reviews in medicinal chemistry. May 2014;14(5):444-452.
20. Pohanka M et al. Ascorbic acid: an old player with a broad impact on body physiology including oxidative stress suppression and immunomodulation: a review. Mini reviews in medicinal chemistry. Jan 2012;12(1):35-43.
21. Holmannova D et al. [Vitamin C and its physiological role with respect to the components of the immune system]. Vnitrni lekarstvi. Oct 2012;58(10):743-749.
22. Uchio R et al. High dietary intake of vitamin C suppresses age-related thymic atrophy and contributes to the maintenance of immune cells in vitamin C-deficient senescence marker protein-30 knockout mice. The British journal of nutrition. Feb 28 2015;113(4):603-609.
23. Hemila H et al. Vitamin C for preventing and treating the common cold. The Cochrane database of systematic reviews. 2013;1:Cd000980.
24. Siqueiros-Cendon T et al. Immunomodulatory effects of lactoferrin. Acta pharmacologica Sinica. 2014;35(5):557-566.
25. Legrand D et al. Lactoferrin structure and functions. Advances in experimental medicine and biology. 2008;606:163-194.
26. Zakharova ET et al. Human apo-lactoferrin as a physiological mimetic of hypoxia stabilizes hypoxia-inducible factor-1 alpha. Biometals: an international journal on the role of metal ions in biology, biochemistry, and medicine. Dec 2012;25(6):1247-1259.
27. Luna-Castro S et al. Effect of bovine apo-lactoferrin on the growth and virulence of Actinobacillus pleuropneumoniae. Biometals: an international journal on the role of metal ions in biology, biochemistry, and medicine. Oct 2014;27(5):891-903.
28. Valenti P et al. Lactoferrin: an important host defence against microbial and viral attack. Cellular and molecular life sciences: CMLS. Nov 2005;62(22):2576-2587.
29. Caccavo D et al. Antimicrobial and immunoregulatory functions of lactoferrin and its potential therapeutic application. J Endotoxin Res. 2002;8(6):403-417.
30. Zagulski T et al. Lactoferrin can protect mice against a lethal dose of Escherichia coli in experimental infection in vivo. British journal of experimental pathology. Dec 1989;70(6):697-704.
31. Krissansen GW. Emerging health properties of whey proteins and their clinical implications. Journal of the American College of Nutrition. Dec 2007;26(6):713s-723s.
32. Rusu D et al. A bovine whey protein extract can enhance innate immunity by priming normal human blood neutrophils. The Journal of nutrition. Feb 2009;139(2):386-393.
33. Kloek J et al. A whey-based glutathione-enhancing diet decreases allergen-induced airway contraction in a guinea-pig model of asthma. The British journal of nutrition. May 2011;105(10):1465-1470.
34. Kent KD et al. Effect of whey protein isolate on intracellular glutathione and oxidant-induced cell death in human prostate epithelial cells. Toxicol In Vitro. Feb 2003;17(1):27-33.
35. Freeman SL et al. Dairy proteins and the response to pneumovax in senior citizens: a randomized, double-blind, placebo-controlled pilot study. Annals of the New York Academy of Sciences. Mar 2010;1190:97-103.
36. Jensen GS et al. A novel extract from bovine colostrum whey supports innate immune functions. II. Rapid changes in cellular immune function in humans. Preventive medicine. May 2012;54 Suppl:S124-129.
37. Batra P et al. Probing Lingzhi or Reishi medicinal mushroom Ganoderma lucidum (higher Basidiomycetes): a bitter mushroom with amazing health benefits. International journal of medicinal mushrooms. 2013;15(2):127-143.
38. Jin X et al. Ganoderma lucidum (Reishi mushroom) for cancer treatment. The Cochrane database of systematic reviews. 2012;6:CD007731.
39. Xu Z et al. Ganoderma lucidum polysaccharides: immunomodulation and potential anti-tumor activities. The American journal of Chinese medicine. 2011;39(1):15-27.
40. Avtonomova AV et al. [Antiviral properties of basidiomycetes metabolites]. Antibiotiki i khimioterapiia = Antibiotics and chemoterapy [sic] / Ministerstvo meditsinskoi i mikrobiologicheskoi promyshlennosti SSSR. 2014;59(7-8):41-48.
41. Li YQ et al. Anti-hepatitis B activities of ganoderic acid from Ganoderma lucidum. Biotechnology letters. Jun 2006;28(11):837-841.
42. Ma B et al. Triterpenoids from the spores of Ganoderma lucidum. North American journal of medical sciences. Nov 2011;3(11):495-498.
43. Vazirian M et al. Antimicrobial effect of the Lingzhi or Reishi medicinal mushroom, Ganoderma lucidum (higher Basidiomycetes) and its main compounds. International journal of medicinal mushrooms. 2014;16(1):77-84.
44. Wu Z et al. ReishiMax extends the lifespan of mice: A preliminary report. The FASEB Journal. 2011;25(1 Supplement):601.602.
45. Chen W et al. Synergy of Ganoderma lucidum Extract ReishiMax and Green Tea Polyphenols Tegreen in Anti-Cancer in a S180-inoculation model. The FASEB Journal. 2007;21(6):A1100.
46. Buford TW et al. Impact of DHEA(S) and cortisol on immune function in aging: a brief review. Applied physiology, nutrition, and metabolism = Physiologie appliquee, nutrition et metabolisme. Jun 2008;33(3):429-433.
47. Weksler ME. Immune senescence and adrenal steroids: immune dysregulation and the action of dehydroepiandrosterone (DHEA) in old animals. Eur J Clin Pharmacol. 1993;45 Suppl 1:S21-23; discussion S43-24.
48. Kroll J. Dehydroepiandrosterone, molecular chaperones and the epigenetics of primate longevity. Rejuvenation Res. Feb 23 2015.
49. UMMC. University of Maryland Medical Center. Dehydroepiandrosterone. https://umm.edu/health/medical/altmed/supplement/dehydroepiandrosterone. 6/26/2014.
50. Khorram O et al. Activation of immune function by dehydroepiandrosterone (DHEA) in age-advanced men. J Gerontol A Biol Sci Med Sci. Jan 1997;52(1):M1-7.
51. Prall SP et al. Dehydroepiandrosterone and multiple measures of functional immunity in young adults. American journal of human biology: the official journal of the Human Biology Council. Nov-Dec 2015;27(6):877-880.
52. Straub RH et al. Serum dehydroepiandrosterone (DHEA) and DHEA sulfate are negatively correlated with serum interleukin-6 (IL-6), and DHEA inhibits IL-6 secretion from mononuclear cells in man in vitro: possible link between endocrinosenescence and immunosenescence. The Journal of clinical endocrinology and metabolism. Jun 1998;83(6):2012-2017.
53. Varadhan R et al. Simple Biologically Informed Inflammatory Index of Two Serum Cytokines Predicts 10 Year All-Cause Mortality in Older Adults. The Journals of Gerontology Series A: Biological Sciences and Medical Sciences. 2014;69A(2):165-173.
54. Danenberg HD et al. Dehydroepiandrosterone (DHEA) treatment reverses the impaired immune response of old mice to influenza vaccination and protects from influenza infection. Vaccine. 1995;13(15):1445-1448.
55. Corsini E et al. Age-related decline in RACK-1 expression in human leukocytes is correlated to plasma levels of dehydroepiandrosterone. Journal of leukocyte biology. Feb 2005;77(2):247-256.
56. Buoso E et al. Opposing effects of cortisol and dehydroepiandrosterone on the expression of the receptor for Activated C Kinase 1: implications in immunosenescence. Experimental gerontology. Nov 2011;46(11):877-883.
57. Chan GC et al. The effects of beta-glucan on human immune and cancer cells. Journal of hematology & oncology. 2009;2:25.
58. Karumuthil-Melethil S et al. Fungal beta-glucan, a Dectin-1 ligand, promotes protection from type 1 diabetes by inducing regulatory innate immune response. Journal of immunology (Baltimore, Md.: 1950). Oct 1 2014;193(7):3308-3321.
59. Aleem E. beta-Glucans and their applications in cancer therapy: focus on human studies. Anti-cancer agents in medicinal chemistry. Jun 2013;13(5):709-719.
60. Vannucci L et al. Immunostimulatory properties and antitumor activities of glucans (Review). International journal of oncology. Aug 2013;43(2):357-364.
61. Chen J et al. Medicinal importance of fungal beta-(1-->3), (1-->6)-glucans. Mycological research. Jun 2007;111(Pt 6):635-652.
62. Dalonso N et al. beta-(1-->3),(1-->6)-Glucans: medicinal activities, characterization, biosynthesis and new horizons. Appl Microbiol Biotechnol. Oct 2015;99(19):7893-7906.
63. Liu Q et al. Tumor-Educated CD11bhighIalow Regulatory Dendritic Cells Suppress T Cell Response through Arginase I. The Journal of Immunology. May 15, 2009 2009;182(10):6207-6216.
64. Ning Y et al. beta-glucan restores tumor-educated dendritic cell maturation to enhance antitumor immune responses. International journal of cancer. Journal international du cancer. Jun 1 2016;138(11):2713-2723.
65. Perez-Martinez A et al. Arabinoxylan rice bran (MGN-3/Biobran) enhances natural killer cell-mediated cytotoxicity against neuroblastoma in vitro and in vivo. Cytotherapy. May 2015;17(5):601-612.
66. Cholujova D et al. MGN-3 arabinoxylan rice bran modulates innate immunity in multiple myeloma patients. Cancer immunology, immunotherapy: CII. Mar 2013;62(3):437-445.
67. Weiskopf D et al. The aging of the immune system. Transpl Int. Nov 2009;22(11):1041-1050.
68. Choi JY et al. Dietary supplementation with rice bran fermented with Lentinus edodes increases interferon-gamma activity without causing adverse effects: a randomized, double-blind, placebo-controlled, parallel-group study. Nutrition journal. 2014;13:35.
69. Maeda H et al. Oral administration of hydrolyzed rice bran prevents the common cold syndrome in the elderly based on its immunomodulatory action. BioFactors (Oxford, England). 2004;21(1-4):185-187.
70. Kim HY et al. A polysaccharide extracted from rice bran fermented with Lentinus edodes enhances natural killer cell activity and exhibits anticancer effects. Journal of medicinal food. Mar 2007;10(1):25-31.
71. Ghoneum M et al. Modified arabinoxylan from rice bran, MGN-3/biobran, sensitizes metastatic breast cancer cells to paclitaxel in vitro. Anticancer research. Jan 2014;34(1):81-87.
72. Ghoneum M et al. Arabinoxylan rice bran (MGN-3/Biobran) provides protection against whole-body gamma-irradiation in mice via restoration of hematopoietic tissues. Journal of radiation research. May 2013;54(3):419-429.
73. Cholujova D et al. BioBran-augmented maturation of human monocyte-derived dendritic cells. Neoplasma. 2009;56(2):89-95.
74. Ghoneum M et al. Synergistic apoptotic effect of arabinoxylan rice bran (MGN-3/Biobran) and curcumin (turmeric) on human multiple myeloma cell line U266 in vitro. Neoplasma. 2011;58(2):118-123.
75. Ghoneum M et al. Augmentation of macrophage phagocytosis by modified arabinoxylan rice bran (MGN-3/biobran). International journal of immunopathology and pharmacology. Sep-Dec 2004;17(3):283-292.
76. Ghoneum M et al. Mgn-3/biobran enhances generation of cytotoxic CD8+ T cells via upregulation of dec-205 expression on dendritic cells. International journal of immunopathology and pharmacology. Oct-Dec 2014;27(4):523-530.
77. Sheeja K et al. Andrographis paniculata downregulates proinflammatory cytokine production and augments cell mediated immune response in metastatic tumor-bearing mice. Asian Pacific journal of cancer prevention: APJCP. 2010;11(3):723-729.
78. Ji LL et al. Andrograpanin, a compound isolated from anti-inflammatory traditional Chinese medicine Andrographis paniculata, enhances chemokine SDF-1alpha-induced leukocytes chemotaxis. Journal of cellular biochemistry. Aug 1 2005;95(5):970-978.
79. Goronzy JJ et al. Understanding immunosenescence to improve responses to vaccines. Nat Immunol. 2013;14(5):428-436.
80. Grubeck-Loebenstein B et al. Immunosenescence and vaccine failure in the elderly. Aging Clin Exp Res. Jun 2009;21(3):201-209.
81. McElhaney JE et al. The unmet need in the elderly: how immunosenescence, CMV infection, co-morbidities and frailty are a challenge for the development of more effective influenza vaccines. Vaccine. Mar 9 2012;30(12):2060-2067.
82. Xu Y et al. Modulation of immune response in mice immunised with an inactivated Salmonella vaccine and gavaged with Andrographis paniculata extract or andrographolide. International immunopharmacology. Apr 2007;7(4):515-523.
83. Ebrahimi M et al. Purified Protein Fraction of Garlic Extract Modulates Cellular Immune Response against Breast Transplanted Tumors in BALB/c Mice Model. Cell journal. Spring 2013;15(1):65-75.
84. Purev U et al. Individual differences on immunostimulatory activity of raw and black garlic extract in human primary immune cells. Immunopharmacology and immunotoxicology. Aug 2012;34(4):651-660.
85. Kyo E et al. Immunomodulatory effects of aged garlic extract. The Journal of nutrition. Mar 2001;131(3s):1075s-1079s.
86. Ried K. Garlic Lowers Blood Pressure in Hypertensive Individuals, Regulates Serum Cholesterol, and Stimulates Immunity: An Updated Meta-analysis and Review. The Journal of nutrition. Feb 2016;146(2):389s-396s.
87. Percival SS. Aged Garlic Extract Modifies Human Immunity. The Journal of nutrition. Feb 2016;146(2):433s-436s.
88. Ghazanfari T et al. Garlic induces a shift in cytokine pattern in Leishmania major-infected BALB/c mice. Scandinavian journal of immunology. Nov 2000;52(5):491-495.
89. Kyo E et al. Prevention of psychological stress-induced immune suppression by aged garlic extract. Phytomedicine: international journal of phytotherapy and phytopharmacology. Nov 1999;6(5):325-330.
90. Jin JO et al. Fucoidan can function as an adjuvant in vivo to enhance dendritic cell maturation and function and promote antigen-specific T cell immune responses. PloS one. 2014;9(6):e99396.
91. Negishi H et al. Supplementation of elderly Japanese men and women with fucoidan from seaweed increases immune responses to seasonal influenza vaccination. The Journal of nutrition. Nov 2013;143(11):1794-1798.
92. Lee JH et al. The sulfated polysaccharide fucoidan rescues senescence of endothelial colony-forming cells for ischemic repair. Stem cells (Dayton, Ohio). Jun 2015;33(6):1939-1951.
93. Aranha I et al. Immunostimulatory properties of the major protein from the stem of the Ayurvedic medicinal herb, guduchi (Tinospora cordifolia). Journal of ethnopharmacology. Jan 31 2012;139(2):366-372.
94. Bala M et al. Validation of ethnomedicinal potential of Tinospora cordifolia for anticancer and immunomodulatory activities and quantification of bioactive molecules by HPTLC. Journal of ethnopharmacology. Dec 4 2015;175:131-137.
95. Bala M et al. Chemical prospection of important ayurvedic plant Tinospora cordifolia by UPLC-DAD-ESI-QTOF-MS/MS and NMR. Natural product communications.Jan 2015;10(1):43-48.
96. Nair PK et al. Immune stimulating properties of a novel polysaccharide from the medicinal plant Tinospora cordifolia. International immunopharmacology. Dec 15 2004;4(13):1645-1659.
97. Pandey VK et al. G1-4A, a polysaccharide from Tinospora cordifolia induces peroxynitrite dependent killer dendritic cell (KDC) activity against tumor cells. International immunopharmacology. Dec 2014;23(2):480-488.
98. Rege N et al. Immunotherapy with Tinospora cordifolia: a new lead in the management of obstructive jaundice. Indian journal of gastroenterology: official journal of the Indian Society of Gastroenterology. Jan 1993;12(1):5-8.
99. Sannegowda KM et al. Tinospora cordifolia inhibits autoimmune arthritis by regulating key immune mediators of inflammation and bone damage. International journal of immunopathology and pharmacology. Dec 2015;28(4):521-531.
美国医学图书馆
www.nlm.nih.gov
维基百科-免疫衰老
https://en.wikipedia.org/wiki/Immunosenescence
《美国科学院院报》
www.pnas.org
美国国立公众健康网
https://medlineplus.gov
免责声明和安全信息
概述
进入老年期免疫功能不断下降,越来越容易受到各种感染或对疫苗反应差,这大多与免疫衰老有关。免疫系统衰老是机体衰老的重要组成部分,是导致生命缩短的自体免疫病和恶性肿瘤或癌症等衰老性疾病的主因。研究表明,一些天然物质可以减缓或逆转免疫衰老,包括抑制胸腺萎缩,提高T细胞亚群量、增强自然杀伤细胞(NK)活性等,以及调整饮食和健康生活方式,有助于恢复年轻状态的免疫功能,提高老年期生命质量。衰老导致免疫下降
年龄老化导致免疫力下降,例如:老年感冒恢复期长或引起严重的并发症,老年人接种疫苗的抗体反应差;与低度炎症相关的老化性疾病,如心脑血管病、糖尿病和癌症等。分析认为,免疫衰老是老年免疫功能下降的主因:- 幼稚T细胞衰减:幼稚T细胞(Naïve T cells,也称初始T细胞)起源于骨髓中的前体细胞并在胸腺中成熟,它们尚未被抗原暴露和激活,故又称为未致敏T细胞。因此,激活幼稚T细胞可识别和应对新的挑战。但是,需要大量的幼稚T细胞来启动对新抗原的免疫应答,例如流感病毒的新变种、新疫苗接种抗原和癌细胞等。大约70岁开始,幼稚T细胞普遍下降,而且,老年人的幼稚T细胞比青年人表现出多种功能缺陷,包括增殖力受损、对新抗原免疫应答耐力降低等。这会损害抵御病原物,降低疫苗效力,并增加患癌风险等。
- 衰老记忆T细胞增加:记忆T细胞是在最初与抗原相遇后产生的特化T细胞,其在暴露结束后持续很长时间。再次暴露于抗原后,记忆T细胞识别抗原并发出快速而有力的反应。随着时间的推移,暴露于多种抗原会增加身体保护记忆T细胞的数量。然而,来自老年人的记忆T细胞通常会衰老,这意味着它们失去了增殖能力并且已经失去应有活性。
- 尽管不能分裂,衰老细胞仍然活跃,分泌高水平的促炎分子,例如肿瘤坏死因子-α和白细胞介素-6。衰老T细胞引发的慢性炎症可能是心血管疾病和其他慢性衰老疾病的一个促成因素。还有证据表明,衰老的记忆T细胞可能抑制其他类型的免疫细胞。
- 记忆T细胞的衰老可能部分地导致终生暴露于常见的病毒感染,例如巨细胞病毒(CMV)和爱泼斯坦病毒(EBV)。这些病毒在体内保持无活性数十年,引发记忆细胞和其他适应性免疫细胞的慢性低强度反应。除了诱导慢性炎症外,这种长期低水平的T细胞活化最终可能导致T细胞功能障碍和衰老。
- NK细胞活性减少:NK细胞活性与健康长寿有关,而NK细胞功能降低与感染、动脉粥样硬化和流感疫苗抗体反应降低,及导致疾病和死亡增加有关。
NK细胞功能随着年龄的增长而降低。活化的NK细胞分泌免疫调节细胞因子,但来自老年人的活化NK细胞产生的细胞因子比来自年轻人的NK细胞少。伴随人类衰老的NK细胞功能下降与老年人细菌和真菌感染的发生率增加有关。
- 胸腺萎缩:这是免疫衰老最显著的变化之一。胸腺功能随着年龄的增长而降低,其幼稚T细胞产生减少。随着记忆T细胞的积累,这有助于T细胞群向记忆T细胞优势的转变。因此,应对包括疫苗在内的新免疫挑战的能力受到影响,对感染、自体免疫疾病和癌症的易感性也增加。
- 过量产生白细胞介素-6(IL-6):免疫衰老与高水平的炎性细胞因子白细胞介素-6(IL-6)有关。研究表明,在健康的百岁老人中IL-6水平较低;IL-6升高与多种老化性慢性病显著相关,包括心脑血管病、痴呆、体弱和癌症等。
- 巨细胞病毒(CMV):这是人类疱疹病毒家族的一员,感染很常见,大多数人没有或意识不到CMV感染症状。与许多疱疹病毒一样,CMV存在于在整个生命过程中,但大部分时间都处于潜伏状态。在免疫系统受损人群中,CMV可以被重新激活并引起严重疾病,包括癌症等。
CMV可能是老年个体特别需要关注的问题,高于90%的75岁以上的人患有持续的CMV感染。许多研究表明,持续性CMV感染与免疫衰老、心血管疾病、体质虚弱和死亡有关。 CMV在免疫衰老背景下的相关性似乎取决于控制病毒所需的免疫能力,并可能因人而异。在一些个体中,长期CMV感染可能引发致力于CMV的记忆T细胞的扩增和幼稚T细胞群的收缩。幼稚T细胞的减少可能削弱免疫系统对与潜在有害微生物相关的新抗原以及疫苗中新抗原的反应能力。
了解免疫系统
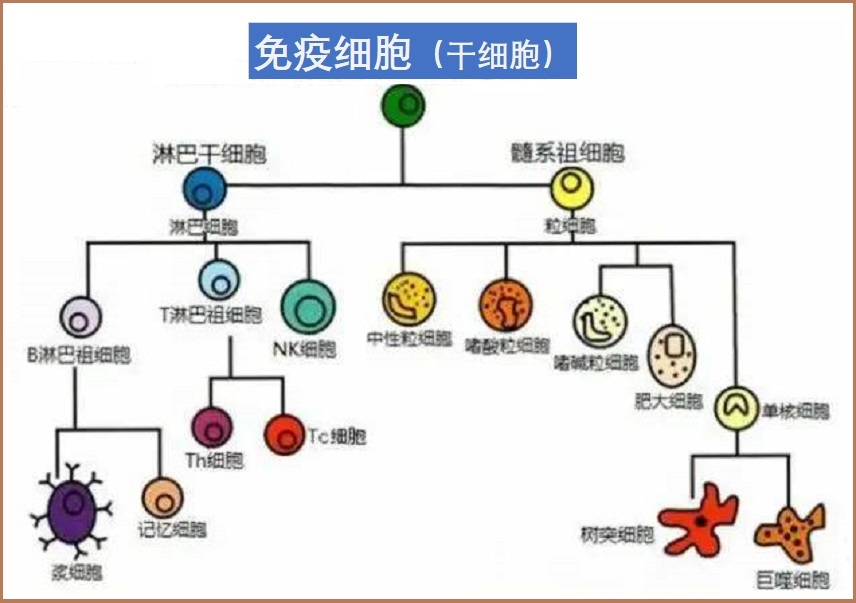
免疫系统包括先天性免疫和适应性免疫,二者之间密切相关。1.先天性免疫(或固有免疫):它是人体对外来和潜在有害物质的第一反应系统,免疫反应迅速,可以非特异性地攻击引发免疫反应的抗原物。其关键组成部分包括如下:
- 物理和化学屏障:如皮肤及其分泌物,呼吸道内壁、胃肠道粘膜以及胃酸等。
- 吞噬性白细胞:如中性粒细胞、巨噬细胞、单核细胞和树突细胞等,吞噬和破坏入侵者并激活适应性免疫系统应答。
- 自然杀伤细胞(NK细胞):这些特异性免疫细胞迅速起作用以破坏异常细胞,特别是肿瘤细胞和感染病毒细胞。
- 急性期蛋白:参与先天免疫和适应性免疫。一些急性期蛋白,包括C-反应蛋白和纤维蛋白原,是临床常用的炎症标志物。
2.适应性免疫(或获得性免疫):在出生后人体逐步建立起来,通过针对特定外来抗原产生抗体而发挥免疫作用。如果先天免御系统没有消除威胁,那么下一级防御就是适应性免疫,其对个体抗原做出特异性反应。获得性免疫具有记忆能力,如注射麻疹疫苗后,就不会再发生麻疹感染。适应性免疫包括抗体和细胞介导的免疫:
- 抗体介导的免疫:由免疫细胞(B细胞)产生并分泌到血液和其他组织中的抗体,识别并结合产生在病毒、细菌、真菌或过敏原表面的特定抗原(如在自体免疫条件下的自身细胞),以消除它们或标记它们被其他免疫细胞破坏。
- 细胞介导的免疫:依赖于T细胞,可对感染的细胞以及已经吞噬有害微生物的吞噬细胞发生作用。胸腺负责产生成熟的T细胞,因年龄老化导致的胸腺萎缩在免疫衰老中起主要作用。
参与细胞介导免疫的T细胞类型为辅助性T细胞、细胞毒性T细胞和调节性T细胞:
- 辅助性T细胞:辅助T细胞增强其他免疫细胞的功能。它们促进B细胞产生抗体,并帮助其他免疫细胞识别、杀死微生物和感染细胞。
- 细胞毒性T细胞:与NK细胞一样,细胞毒性T细胞直接攻击并破坏外来细胞,感染细胞和异常细胞,包括癌细胞和非自身细胞。
- 调节性T细胞:调节性T细胞通常控制或终止对入侵者的免疫应答,最小化组织损伤并帮助抵抗免疫系统过度反应的状况,例如自身免疫疾病和过敏。
附1. 衰老与调节性T细胞:最新研究表明,调节性T细胞可能在免疫衰老中发挥作用:
- 某些类型的调节性T细胞似乎随着年龄的增长而累积,并且可能削弱对病原体或恶性细胞的免疫应答。与此同时,似乎其他类型的调节性T细胞的数量保持不变甚至下降。此外,调节性T细胞的功能可能随年龄而变化。因此,平衡且维持功能正常的调节性T细胞矩阵似乎是必要的,以避免在抑制慢性炎症的同时保持免疫能力并防止感染、癌变。
- 总体而言,调节性T细胞在免疫衰老背景下的影响不能明确说明,并且可能因个体而异。例如,有自身免疫性疾病病史的人可能会受益于增加的调节性T细胞数量或活性,而易患感染或癌症但没有自身免疫性疾病史的人可能会受益于降低调节性T细胞活性。
附2. 肠道菌群与免疫:人体大约有30万亿细菌,其中约70%定植于肠道粘膜。肠道菌群失衡可增加炎症反应,引起感染及促进疾病发展,不良饮食、有害微生物,以及抗生素、某些药物和毒素等可破坏菌落平衡。此外,肠道微生物群体的变化也可能与衰老有关。
- 热量限制(CR)是目前普遍接受的有助于延缓衰老的有效途径。CR的免疫增强与肠道有益菌群改善有关。此外,CR也减少了肠道摄取的免疫反应物(抗原)量,降低免疫系统负荷。
- 补充益生菌有助于增强老年免疫功能,可降低传染病的发生频率和严重程度,有关临床对照试验表明,补充益生菌(植物乳杆菌、鼠李糖乳杆菌、枯草芽孢杆菌和乳双歧杆菌)、益生元和乳铁蛋白,减少了寒冷季节老年人呼吸道疾病的发病率,严重程度和持续时间。
评估免疫功能指标
- 白细胞计数:异常水平可能存在感染、血癌或免疫系统疾病的征兆。
- 巨细胞病毒(CMV)IgM和IgG:帮助诊断CMV感染或再激活; IgM CMV阳性表示最近有CMV感染或重新激活; 阳性CMV IgG表示已暴露于CMV,但一次测试不能区分过去或最近的感染。
- 爱泼斯坦巴尔病毒(EBV)抗体:评估持续存在的EBV感染,这可能与免疫衰老有关。
- 人类疱疹病毒6型(HHV-6)IgG,IgM:评估HHV-6的总抗体。
- 自然杀伤细胞功能:评估NK细胞的杀伤能力。
- 自然杀伤(NK)细胞表面抗原(CD3-CD56+标记分析):确定血液循环中NK细胞的水平。
- 补体C3和C4:低水平的C3和C4可能与系统性红斑狼疮等自身免疫性疾病有关。
- C-反应蛋白:高度敏感的炎症标志物,表明免疫激活,可能是由于癌症、感染、损伤或自身免疫性疾病引起的;与心血管病风险相关。
- 皮质醇和脱氢表雄酮硫酸盐(DHEA-S):皮质醇具有免疫抑制作用,而DHEA刺激免疫功能;这些激素之间的不平衡可能导致免疫失调。
- 细胞因子例如TNF-α和白介素IL-1beta,IL-6,IL-8:炎症反应关键介质的蛋白质。
- 抗核抗体:在一些自身免疫性疾病中升高。
- 免疫球蛋白IgA,IgG,IgM:在一些自身免疫性疾病、多发性骨髓瘤、急性和慢性感染中升高;在免疫缺陷方面减少。
- T淋巴细胞辅助/抑制状态:可能有助于评估免疫缺陷。
饮食、生活方式与免疫衰老
- 热量限制:原则是减少总热量摄入,但保持最佳营养。最好通过食用主要由低热量、营养密集的饮食来完成,如蔬菜、水果、豆类、坚果,以及全谷物;限制动物产品的摄入量;并避免高热量、营养不良的食物。
- 长期热量限制会导致人体代谢变化,从而降低许多与年龄相关的疾病(包括2型糖尿病,心血管疾病和癌症)的风险。在一项临床研究中,6个月的热量限制显著提高了T细胞对外源抗原反应的能力。
- 热量限制饮食在动物实验中已被证明可以改善免疫活性、刺激胸腺功能、T细胞增殖和功能;可延长寿命并延缓衰老,赋予T细胞更年轻的特征。
了解更多相关内容可参与本网站专文:热量限制与抗衰老 >>
- 地中海饮食:其主要包含水果、蔬菜、橄榄油、全谷物、坚果和种子,以及适量的海鱼、家禽、奶酪和鸡蛋,还有限量的红肉、腌制肉制品和精制糖类食物;佐餐配以适量红酒。这种饮食在地中海地区自古以来就存在,已被证明可以预防多种与年龄和炎症相关的疾病,包括年龄相关性肥胖、糖尿病、动脉粥样硬化、神经退行性疾病和癌症等。
- 2014年对17项临床试验的综述,对地中海饮食模式的更大依从性与白细胞介素6(IL-6)和高敏C反应蛋白(两种重要的炎症标志物)水平显着降低相关。
- 运动锻炼:研究表明,适度运动可以对抗免疫衰老。在一项久坐不动的老年群体研究中,随机接受10个月锻炼的存在中度心血管病的参与者,与仅从事灵活性和平衡练习的老年人相比,抗体对流感疫苗的反应有所改善。在另一项针对老年妇女研究中,两年的常规体力活动增加了白介素2(IL-2)的产生,后者是免疫反应的重要调节因子,通常随着年龄的增长而降低。2011年的一项研究发现,有氧运动与衰老T细胞的减少有关。
了解更多相关内容可参与本网站专文:运动促进健康 >>
-
压力管理:通过抑制免疫和促进持续的全身性炎症水平,慢性压力导致先天性和适应性免疫应答的失调。当压力削弱免疫功能时,可允许诸如巨细胞病毒等潜伏病毒逃避免疫系统监控,潜伏病毒的不断再激活可以加剧免疫系统紧张、紊乱。慢性压力诱导的肾上腺激素(皮质醇)升高似乎有助于免疫衰老。事实上,皮质醇与另一种肾上腺素—脱氢表雄酮(DHEA)的比例失衡可能是免疫衰老的重要决定因素。
- 在对早期乳腺癌患者的研究中,压力管理干预已被证明可以改善细胞免疫功能并逆转循环免疫细胞中的促炎基因表达;类风湿性关节炎患者的压力管理训练导致应激诱导的白介素8(IL-8)—炎性因子水平降低。
了解更多相关内容可参与本网站专文:压力管理 >>
-
睡眠管理:已知睡眠不足会削弱免疫功能,增加对呼吸道的易感性包括普通感冒,长期睡眠不足可能导致死亡风险增加。睡眠剥夺与皮质醇水平升高以及白天炎症细胞因子水平升高有关,包括白介素-1、白介素-6和肿瘤坏死因子-α。
- 一项针对61-86岁个体的研究发现,即使是一夜的部分睡眠剥夺也诱导了与生物衰老相关的基因激活。
- 睡眠不良可影响包括调节性T细胞和适应性免疫系统的其他细胞功能变化,以及NK细胞、T细胞和B细胞数量的减少。
- 研究显示睡眠减少会改变抗体与细胞介导的免疫平衡。
了解更多相关内容可参与本网站专文:睡眠障碍 >>
营养与草本综合干预
以下是基于循证医学和营养学有关文献综合的结果。有助于防控免疫衰老的营养和草本补充剂,主要包括如下:
1.锌:
锌是一种重要的微量矿物质,对健康的免疫功能至关重要。锌缺乏在老年人中很常见,并导致免疫功能的变化,类似于免疫衰老1,2。与缺锌相关的免疫改变包括胸腺功能下降、对疫苗的抗体反应降低以及吞噬细胞和NK细胞功能受损2,3。
在一项针对健康老年志愿者的研究中,与安慰剂相比,一年内每天摄入45mg锌可使感染发生率降低67%。服用锌的患者的肿瘤坏死因子α(一种炎症细胞因子)水平也大大降低4。在一项针对养老院老年人的研究中,与缺锌的人相比,锌水平正常的居民肺炎的发病率明显较低。锌充足的个体肺炎持续时间更短,抗生素使用率降低50%,全因死亡率更低5。一项针对老年人的对照临床试验显示,在六个月内每天补充45mg锌可降低血浆炎症标志物,包括IL-6和C反应蛋白6。
将锌与其他重要的维生素和矿物质结合也可能有助于免疫功能。在一项随机对照试验中,招募了42名年龄在55岁至75岁之间的受试者,与服用安慰剂的人相比,服用含有10mg锌和1000mg维生素C以及其他维生素和矿物质的复合维生素/矿物质补充剂12周的人自报患病天数更少,症状也不那么严重。使用补充剂后,病假天数减少了近65%7。
2.维生素E:
充足的维生素E对维持有效的免疫功能至关重要。事实上,各种动物研究表明,维生素E缺乏会引发免疫抑制。临床证据表明,补充维生素E可以增加对感染的抵抗力,尤其是在老年人中8,9。
在一项针对老年男性和女性的研究中,每天补充200mg维生素E可显著增强免疫参数,包括中性粒细胞、T细胞、B细胞和NK细胞功能,使其值接近年轻健康成年人10。
增加维生素E的摄入量已被证明可以恢复与衰老相关的T细胞功能的下降。这种T细胞功能的改善源于维生素E对T细胞的直接影响以及对前列腺素E2的抑制,前列腺素E2是炎症介质和T细胞抑制剂9,11。在小鼠模型中,补充维生素E逆转了与年龄相关的幼稚T细胞功能下降12。
3. N-乙酰半胱氨酸:
NAC是含硫氨基酸半胱氨酸的一种形式,它是谷胱甘肽的前体,谷胱甘肽是代谢解毒的重要促进剂13-15。谷胱甘肽在调节炎症反应中起着关键作用,尤其是在肺部。它对某些免疫功能至关重要,包括T细胞的增殖以及中性粒细胞和树突状细胞的细胞杀伤活性。谷胱甘肽细胞水平的降低与感染易感性的增加有关16。
在一项针对262名流感和流感样疾病高危人群的对照临床试验中,六个月内每天两次600mg的NAC补充剂显著降低了流感和流感症状的频率和严重程度,如咳嗽、喉咙痛、头痛以及肌肉和关节疼痛。NAC预防流感症状的能力在冬季尤为明显。在研究期间流感病毒感染检测呈阳性的人中,NAC组只有25%出现症状性疾病,而安慰剂组为79%17。透析患者在八周内使用相同的NAC剂量,导致炎症标志物水平显著降低,包括C反应蛋白、肿瘤坏死因子α和IL-618。
4.维生素C:
维生素C支持先天免疫系统和适应性免疫系统的功能,在防御细菌和病毒方面发挥着重要作用。除了刺激免疫力外,维生素C似乎还可以抑制过度的免疫活性,可能部分是通过干扰炎症细胞因子的合成19-21。
新增加的证据表明,随着年龄的增长,补充维生素C可能有助于维持免疫功能。在维生素C缺乏和过早衰老的小鼠模型中,补充较高剂量的维生素C(相当于79.5kg体重的人每天大约1300mg)与较低剂量(相当于79.5kg体重的人每天约130mg)进行了比较。一年后,接受高剂量维生素C的小鼠比接受低剂量维生素C小鼠表现出更好的胸腺保存和更大的免疫细胞计数22。
一项对安慰剂对照试验的大型分析结果表明,补充维生素C可以缩短感冒的持续时间,成人和儿童分别减少8%和14%。此外,该分析发现,维生素C补充剂将马拉松运动员等剧烈体力消耗人群的感冒发病率降低了一半23。
5.乳铁蛋白:
乳铁蛋白是一种铁结合蛋白,存在于身体分泌物中,包括母乳、唾液、眼泪、鼻腔分泌物、肠液以及中性粒细胞中。乳铁蛋白的抗菌作用包括破坏微生物细胞膜,结合和分离铁,而铁是几乎所有细菌生长和繁殖所需的24,25。无铁形式的乳铁蛋白(脱乳铁蛋白)是一种有效的铁结合蛋白,并已被证明具有抗菌作用24,26,27。
乳铁蛋白对包括细菌、病毒、真菌和寄生虫在内的多种微生物具有直接的抗菌活性25,28,29。在一项动物研究中,69%的经静脉注射乳铁蛋白预处理的小鼠在给予致命剂量的有毒大肠杆菌后存活了30天,而只有4%的对照小鼠存活30。
6.乳清蛋白:
乳清是奶酪制作过程中从凝乳中分离出来的液体。源自乳清的产品已证明具有免疫调节特性31,32。乳清蛋白特别富含参与谷胱甘肽合成的前体氨基酸,谷胱甘肽是一种具有抗炎特性的强大自由基清除剂。谷胱甘肽对先天免疫和适应性免疫都至关重要31,33,34。
一项初步研究比较了乳清蛋白和大豆蛋白对17名健康老年人疫苗反应性的影响35。参与者被随机分配在四周内食用乳清蛋白或大豆蛋白。然后,他们接种了肺炎球菌疫苗,并在接种后继续补充蛋白质四周。与接受大豆蛋白的人相比,接受乳清蛋白的人对14种肺炎球菌中的12种表现出更强的抗体反应,其中包括四种最有害的细菌。研究人员得出结论,“补充乳清蛋白是一种很有前途的补充剂,可以刺激老年人对疫苗的免疫反应,并可能抵消(免疫衰老),同时需要进行更大规模的研究。”
在另一项针对12名健康志愿者的临床试验中,单剂量乳清提取物是比安慰剂更有效的免疫激活剂,可以快速提高某些免疫细胞的微生物吞噬活性,并动员新的NK细胞进入循环36。在一项对培养的中性粒细胞的研究中,乳清蛋白提取物没有立竿见影的效果,而是具有启动作用,24小时后提高了中性粒细胞活性32。
7.灵芝:
灵芝是一种药用蘑菇,在亚洲用于免疫系统支持已有2000多年的历史。灵芝含有多糖、三萜和其他潜在的活性化合物。实验室和动物研究表明,灵芝多糖具有免疫调节、抗肿瘤和细胞杀伤作用,这似乎部分源于其影响T细胞、NK细胞和巨噬细胞的能力37-39。
灵芝多糖中的β-葡聚糖已被发现可刺激先天免疫反应和适应性免疫反应38。其他灵芝化合物已证明具有抗病毒特性,包括对单纯疱疹病毒、乙肝病毒和EB病毒的活性。灵芝成分也已被证明能抑制酵母和大肠杆菌的生长40-43。
这些免疫增强作用可能有助于解释一项动物研究的结果,在该研究中,补充灵芝的小鼠比对照小鼠活得更长44。在另一项研究中,含有绿茶提取物和富含多糖和三萜的灵芝提取物的产品刺激免疫细胞的增殖,包括B细胞、T细胞和NK细胞,并抑制小鼠的恶性肿瘤45。
一项对临床对照试验的严格审查发现,癌症患者在化疗和放疗的同时使用灵芝,比未使用灵芝的患者对癌症治疗的积极反应高50%。灵芝还增加了T细胞的几个亚群的百分比,并且可能略微增加了NK细胞的活性。作者得出的结论是,灵芝可以被认为是“考虑到其增强肿瘤反应和刺激宿主免疫的潜力,作为传统治疗的替代辅助手段”38。
8.脱氢表雄酮(DHEA):
DHEA是一种在健康免疫系统功能中发挥主要作用的类固醇激素46,47。DHEA水平随着年龄的增长而显著下降。到80岁时,DHEA水平降至峰值的10-20%48,49。
一项针对平均年龄63岁、血清DHEA-S水平较低的男性的临床试验发现,口服补充DHEA可以迅速纠正DHEA状态。与安慰剂相比,DHEA治疗改善了免疫参数,包括单核细胞水平、B-和T-细胞功能以及NK细胞水平50。在一项针对38名参与者的小型观察性研究中,唾液DHEA水平与唾液杀菌活性呈正相关,后者是衡量先天免疫功能的指标51。另一项观察性研究指出,低水平的DHEA和高水平的IL-6之间存在关联,而IL-6是一种与免疫衰老有关的炎症细胞因子。此外,DHEA还能抑制来自研究参与者的免疫细胞产生IL-652,53。根据一项针对老年小鼠的研究,DHEA也可能增强对流感疫苗的免疫反应54。
DHEA作为皮质醇的平衡物发挥着关键作用。皮质醇是一种具有免疫抑制特性的肾上腺激素,而DHEA可能具有直接的免疫刺激特性:在一项对65岁以上捐献者白细胞的实验室研究中,DHEA治疗逆转了免疫细胞上特异性受体与年龄相关的减少,并提高了免疫细胞的反应性55。尽管DHEA水平随着年龄的增长而急剧下降,但皮质醇水平保持相对恒定,导致这两种激素失衡,这被认为有助于免疫衰老46,56。
10.β-葡聚糖:
β-葡聚糖是一种多糖(碳水化合物),存在于细菌、真菌、谷物(包括燕麦)和藻类的细胞壁中。β-葡聚糖是对灵芝等药用蘑菇的免疫调节益处负责的活性成分之一57-59。
已发现β-葡聚糖可调节免疫活性的多个方面,具有显著的抗肿瘤和抗菌特性60-62。2013年的一项研究综述发现,含有β-葡聚糖的植物提取物提高了癌症患者的存活率和生活质量。这篇综述还发现,β-葡聚糖提取物减少了几种不同形式癌症化疗和放疗的副作用59。
肿瘤细胞通过抑制免疫功能和诱导免疫耐受的机制逃避免疫系统63。一项研究表明,β-葡聚糖可能通过降低受肿瘤信号影响的调节性免疫细胞的抑制功能,帮助克服癌症细胞消除的障碍64。
一些富含β-葡聚糖的药用蘑菇包括:蘑菇菌丝体专利品牌AHCC®,云芝蘑菇等。
9.酶改性米糠:
经酶修饰的米糠是米糠的衍生物,已被证明可以增强免疫细胞,特别是NK细胞的数量和功能65-67。这种经过特殊修饰的米糠是增强免疫的阿拉伯木聚糖的来源68,该多糖已被证明可以预防70至95岁人群的上呼吸道病毒感染69。酶改性米糠的多糖部分也表现出抗菌和抗癌特性70。事实上,几位研究人员提出,酶改性米糠作为癌症的辅助治疗可能是有益的65,71,72。
一系列实验室和动物实验表明,酶改性的米糠提高了几种免疫细胞的活性,包括中性粒细胞、单核细胞、巨噬细胞和树突状细胞73-76。在2013年一项针对多发性骨髓瘤患者的研究中,补充酶改性米糠产品可提高NK细胞活性66。酶改性米糠还使培养的乳腺癌症细胞对化疗药物的易感性增加了100倍以上71。
11.穿心莲:
穿心莲是一种亚洲传统的草药,用于治疗感染、感冒、发烧和炎症。在2010年对荷瘤小鼠的一项研究中,穿心莲及其活性成分之一穿心莲内酯增强了NK细胞和其他免疫细胞破坏癌症细胞的能力77,78。
疫苗有效性降低是免疫衰老的一个突出特征79-81,有证据表明穿心莲可能改善对疫苗的免疫反应。在一项针对小鼠的研究中,口服穿心莲提取物和穿心莲内酯都能增强抗体的产生,并激活免疫细胞以应对沙门氏菌疫苗82。
12.大蒜:
大蒜以其改善心血管危险因素的能力而闻名,它还具有免疫调节和免疫刺激特性,以及抗肿瘤作用83-85。
对已发表的临床试验数据的详细审查发现,大蒜补充剂可以显著减少上呼吸道感染的数量、持续时间和严重程度。这篇综述还发现,大蒜补充剂通过增加巨噬细胞活性、NK细胞数量以及T和B细胞的产生来刺激免疫功能86。在一项临床试验中,120名21-50岁的健康参与者被分配在感冒和流感季节每天使用2.56g陈蒜提取物或安慰剂,持续90天。补充大蒜与降低感冒和流感的严重程度以及增加细胞毒性T细胞和NK细胞的增殖和活性有关87。在动物研究中,大蒜已被证明可以增加抗体的产生,并增强巨噬细胞、细胞毒性T细胞和NK细胞的细胞杀伤活性88。其他动物研究表明,老化的大蒜提取物可以防止与心理压力相关的免疫抑制89。
有趣的是,大蒜也被证明可以抑制与过敏反应相关的过度活跃的免疫反应。来自实验研究的数据表明,陈化大蒜提取物可以减少组胺的释放,并改变参与过敏反应的免疫细胞的功能85。
13.岩藻聚糖:
某些日本人的预期寿命是世界上最长的。经常食用富含岩藻聚糖(Fucoidan,又称褐藻糖胶)的棕色海藻可能有助于他们的长寿。研究表明,褐藻糖胶具有增强免疫、抗炎、抗病毒和抗肿瘤的特性90-92。
2014年一项实验室和动物研究的证据表明,褐藻糖胶可能诱导抗肿瘤免疫活性,并提高实验性抗肿瘤疫苗的有效性。根据他们的发现,研究作者认为褐藻糖胶可能在未来作为抗癌疫苗的一种成分是有用的90。
在一项针对日本老年志愿者的研究中,发现补充褐藻糖胶可以增加对季节性流感疫苗的免疫反应。与安慰剂组相比,服用褐藻糖胶的志愿者在接种流感疫苗五周后,流感病毒特异性抗体水平更高,NK细胞活性增加。这些发现表明,褐藻糖胶可以通过提高疫苗的有效性来降低免疫功能较差的老年人的感染率并预防严重的健康问题91。
14.青牛胆:
青牛胆(Tinospora cordifolia)是一种用于传统阿育吠陀医学的草药,一直是许多科学研究的主题。从青牛胆中分离出了几种增强免疫功能的化学成分93-95。
从青牛胆中提取的多糖特别令人感兴趣。其中一种复合碳水化合物—阿拉伯半乳聚糖,已被证明可以增强树突细胞的成熟和这些细胞杀死癌症细胞的能力。另一种青牛胆多聚糖(α-葡聚糖),显示出激活NK细胞、B细胞和T细胞的能力,导致其肿瘤细胞杀伤功能的剂量依赖性增加96,97。
动物和临床研究已经证明了青牛胆在一系列条件下具有强大的免疫作用。在一项针对免疫功能受抑制的外科患者的随机临床试验中,一半患者单独接受常规护理,一半患者接受常规护理加上青牛胆补剂。青牛胆组的中性粒细胞功能正常化,但在对照组没有。败血症是一种血液感染和手术的严重并发症,在50%的对照组中很明显,但在接受青牛胆治疗的患者中没有一例98。在大鼠中,青牛胆降低了关节炎炎症、骨和软骨损伤,还降低了炎性细胞因子的水平,包括肿瘤坏死因子α和IL-699。
更多可查看其个性化综合干预方案如下:
- 免疫衰老管理(提升免疫细胞数)
- 免疫衰老管理(增强免疫活性)
- 免疫衰老管理(改善疫苗反应)
- 女性免疫维持(55-65岁)
- 女性免疫维持(66-75岁)
- 女性免疫维持(76岁以上)
- 男性免疫维持(60-70岁)
- 男性免疫维持(71-80岁)
- 男性免疫维持(81岁以上)
以及参阅本网如下专文的有关内容:
参考文献:
1. Cabrera AJ. Zinc, aging, and immunosenescence: an overview. Pathobiol Aging Age Relat Dis. 2015;5:25592.
2. Maywald M et al. Zinc homeostasis and immunosenescence. J Trace Elem Med Biol. Jan 2015;29:24-30.
3. Haase H et al. The immune system and the impact of zinc during aging. Immunity & ageing: I & A. 2009;6:9.
4. Prasad AS et al. Zinc supplementation decreases incidence of infections in the elderly: effect of zinc on generation of cytokines and oxidative stress. The American journal of clinical nutrition. Mar 2007;85(3):837-844.
5. Meydani SN et al. Serum zinc and pneumonia in nursing home elderly. The American journal of clinical nutrition. Oct 2007;86(4):1167-1173.
6. Bao B et al. Zinc decreases C-reactive protein, lipid peroxidation, and inflammatory cytokines in elderly subjects: a potential implication of zinc as an atheroprotective agent. The American journal of clinical nutrition. Jun 2010;91(6):1634-1641.
7. Fantacone ML et al. The Effect of a Multivitamin and Mineral Supplement on Immune Function in Healthy Older Adults: A Double-Blind, Randomized, Controlled Trial. Nutrients. 2020;12(8).
8. Wu D et al. Age-associated changes in immune function: impact of vitamin E intervention and the underlying mechanisms. Endocrine, metabolic & immune disorders drug targets. 2014;14(4):283-289.
9. Han SN et al. Impact of vitamin E on immune function and its clinical implications. Expert review of clinical immunology. Jul 2006;2(4):561-567.
10. De la Fuente M et al. Vitamin E ingestion improves several immune functions in elderly men and women. Free radical research. Mar 2008;42(3):272-280.
11. Wu D et al. Age-associated changes in immune and inflammatory responses: impact of vitamin E intervention. J Leukoc Biol. Oct 2008;84(4):900-914.
12. Adolfsson O et al. Vitamin E-enhanced IL-2 production in old mice: naive but not memory T cells show increased cell division cycling and IL-2-producing capacity. Journal of immunology (Baltimore, Md.: 1950). Oct 1 2001;167(7):3809-3817.
13. Brosnan JT et al. The sulfur-containing amino acids: an overview. The Journal of nutrition. Jun 2006;136(6 Suppl):1636s-1640s.
14. Santus P et al. Oxidative stress and respiratory system: pharmacological and clinical reappraisal of N-acetylcysteine. COPD. Dec 2014;11(6):705-717.
15. Millea PJ. N-acetylcysteine: multiple clinical applications. American family physician. Aug 1 2009;80(3):265-269.
16. Ghezzi P. Role of glutathione in immunity and inflammation in the lung. International journal of general medicine. 2011;4:105-113.
17. De Flora S et al. Attenuation of influenza-like symptomatology and improvement of cell-mediated immunity with long-term N-acetylcysteine treatment. The European respiratory journal. Jul 1997;10(7):1535-1541.
18. Purwanto B et al. Effect of oral N-acetylcysteine treatment on immune system in continuous ambulatory peritoneal dialysis patients. Acta medica Indonesiana. Apr 2012;44(2):140-144.
19. Sorice A et al. Ascorbic acid: its role in immune system and chronic inflammation diseases. Mini reviews in medicinal chemistry. May 2014;14(5):444-452.
20. Pohanka M et al. Ascorbic acid: an old player with a broad impact on body physiology including oxidative stress suppression and immunomodulation: a review. Mini reviews in medicinal chemistry. Jan 2012;12(1):35-43.
21. Holmannova D et al. [Vitamin C and its physiological role with respect to the components of the immune system]. Vnitrni lekarstvi. Oct 2012;58(10):743-749.
22. Uchio R et al. High dietary intake of vitamin C suppresses age-related thymic atrophy and contributes to the maintenance of immune cells in vitamin C-deficient senescence marker protein-30 knockout mice. The British journal of nutrition. Feb 28 2015;113(4):603-609.
23. Hemila H et al. Vitamin C for preventing and treating the common cold. The Cochrane database of systematic reviews. 2013;1:Cd000980.
24. Siqueiros-Cendon T et al. Immunomodulatory effects of lactoferrin. Acta pharmacologica Sinica. 2014;35(5):557-566.
25. Legrand D et al. Lactoferrin structure and functions. Advances in experimental medicine and biology. 2008;606:163-194.
26. Zakharova ET et al. Human apo-lactoferrin as a physiological mimetic of hypoxia stabilizes hypoxia-inducible factor-1 alpha. Biometals: an international journal on the role of metal ions in biology, biochemistry, and medicine. Dec 2012;25(6):1247-1259.
27. Luna-Castro S et al. Effect of bovine apo-lactoferrin on the growth and virulence of Actinobacillus pleuropneumoniae. Biometals: an international journal on the role of metal ions in biology, biochemistry, and medicine. Oct 2014;27(5):891-903.
28. Valenti P et al. Lactoferrin: an important host defence against microbial and viral attack. Cellular and molecular life sciences: CMLS. Nov 2005;62(22):2576-2587.
29. Caccavo D et al. Antimicrobial and immunoregulatory functions of lactoferrin and its potential therapeutic application. J Endotoxin Res. 2002;8(6):403-417.
30. Zagulski T et al. Lactoferrin can protect mice against a lethal dose of Escherichia coli in experimental infection in vivo. British journal of experimental pathology. Dec 1989;70(6):697-704.
31. Krissansen GW. Emerging health properties of whey proteins and their clinical implications. Journal of the American College of Nutrition. Dec 2007;26(6):713s-723s.
32. Rusu D et al. A bovine whey protein extract can enhance innate immunity by priming normal human blood neutrophils. The Journal of nutrition. Feb 2009;139(2):386-393.
33. Kloek J et al. A whey-based glutathione-enhancing diet decreases allergen-induced airway contraction in a guinea-pig model of asthma. The British journal of nutrition. May 2011;105(10):1465-1470.
34. Kent KD et al. Effect of whey protein isolate on intracellular glutathione and oxidant-induced cell death in human prostate epithelial cells. Toxicol In Vitro. Feb 2003;17(1):27-33.
35. Freeman SL et al. Dairy proteins and the response to pneumovax in senior citizens: a randomized, double-blind, placebo-controlled pilot study. Annals of the New York Academy of Sciences. Mar 2010;1190:97-103.
36. Jensen GS et al. A novel extract from bovine colostrum whey supports innate immune functions. II. Rapid changes in cellular immune function in humans. Preventive medicine. May 2012;54 Suppl:S124-129.
37. Batra P et al. Probing Lingzhi or Reishi medicinal mushroom Ganoderma lucidum (higher Basidiomycetes): a bitter mushroom with amazing health benefits. International journal of medicinal mushrooms. 2013;15(2):127-143.
38. Jin X et al. Ganoderma lucidum (Reishi mushroom) for cancer treatment. The Cochrane database of systematic reviews. 2012;6:CD007731.
39. Xu Z et al. Ganoderma lucidum polysaccharides: immunomodulation and potential anti-tumor activities. The American journal of Chinese medicine. 2011;39(1):15-27.
40. Avtonomova AV et al. [Antiviral properties of basidiomycetes metabolites]. Antibiotiki i khimioterapiia = Antibiotics and chemoterapy [sic] / Ministerstvo meditsinskoi i mikrobiologicheskoi promyshlennosti SSSR. 2014;59(7-8):41-48.
41. Li YQ et al. Anti-hepatitis B activities of ganoderic acid from Ganoderma lucidum. Biotechnology letters. Jun 2006;28(11):837-841.
42. Ma B et al. Triterpenoids from the spores of Ganoderma lucidum. North American journal of medical sciences. Nov 2011;3(11):495-498.
43. Vazirian M et al. Antimicrobial effect of the Lingzhi or Reishi medicinal mushroom, Ganoderma lucidum (higher Basidiomycetes) and its main compounds. International journal of medicinal mushrooms. 2014;16(1):77-84.
44. Wu Z et al. ReishiMax extends the lifespan of mice: A preliminary report. The FASEB Journal. 2011;25(1 Supplement):601.602.
45. Chen W et al. Synergy of Ganoderma lucidum Extract ReishiMax and Green Tea Polyphenols Tegreen in Anti-Cancer in a S180-inoculation model. The FASEB Journal. 2007;21(6):A1100.
46. Buford TW et al. Impact of DHEA(S) and cortisol on immune function in aging: a brief review. Applied physiology, nutrition, and metabolism = Physiologie appliquee, nutrition et metabolisme. Jun 2008;33(3):429-433.
47. Weksler ME. Immune senescence and adrenal steroids: immune dysregulation and the action of dehydroepiandrosterone (DHEA) in old animals. Eur J Clin Pharmacol. 1993;45 Suppl 1:S21-23; discussion S43-24.
48. Kroll J. Dehydroepiandrosterone, molecular chaperones and the epigenetics of primate longevity. Rejuvenation Res. Feb 23 2015.
49. UMMC. University of Maryland Medical Center. Dehydroepiandrosterone. https://umm.edu/health/medical/altmed/supplement/dehydroepiandrosterone. 6/26/2014.
50. Khorram O et al. Activation of immune function by dehydroepiandrosterone (DHEA) in age-advanced men. J Gerontol A Biol Sci Med Sci. Jan 1997;52(1):M1-7.
51. Prall SP et al. Dehydroepiandrosterone and multiple measures of functional immunity in young adults. American journal of human biology: the official journal of the Human Biology Council. Nov-Dec 2015;27(6):877-880.
52. Straub RH et al. Serum dehydroepiandrosterone (DHEA) and DHEA sulfate are negatively correlated with serum interleukin-6 (IL-6), and DHEA inhibits IL-6 secretion from mononuclear cells in man in vitro: possible link between endocrinosenescence and immunosenescence. The Journal of clinical endocrinology and metabolism. Jun 1998;83(6):2012-2017.
53. Varadhan R et al. Simple Biologically Informed Inflammatory Index of Two Serum Cytokines Predicts 10 Year All-Cause Mortality in Older Adults. The Journals of Gerontology Series A: Biological Sciences and Medical Sciences. 2014;69A(2):165-173.
54. Danenberg HD et al. Dehydroepiandrosterone (DHEA) treatment reverses the impaired immune response of old mice to influenza vaccination and protects from influenza infection. Vaccine. 1995;13(15):1445-1448.
55. Corsini E et al. Age-related decline in RACK-1 expression in human leukocytes is correlated to plasma levels of dehydroepiandrosterone. Journal of leukocyte biology. Feb 2005;77(2):247-256.
56. Buoso E et al. Opposing effects of cortisol and dehydroepiandrosterone on the expression of the receptor for Activated C Kinase 1: implications in immunosenescence. Experimental gerontology. Nov 2011;46(11):877-883.
57. Chan GC et al. The effects of beta-glucan on human immune and cancer cells. Journal of hematology & oncology. 2009;2:25.
58. Karumuthil-Melethil S et al. Fungal beta-glucan, a Dectin-1 ligand, promotes protection from type 1 diabetes by inducing regulatory innate immune response. Journal of immunology (Baltimore, Md.: 1950). Oct 1 2014;193(7):3308-3321.
59. Aleem E. beta-Glucans and their applications in cancer therapy: focus on human studies. Anti-cancer agents in medicinal chemistry. Jun 2013;13(5):709-719.
60. Vannucci L et al. Immunostimulatory properties and antitumor activities of glucans (Review). International journal of oncology. Aug 2013;43(2):357-364.
61. Chen J et al. Medicinal importance of fungal beta-(1-->3), (1-->6)-glucans. Mycological research. Jun 2007;111(Pt 6):635-652.
62. Dalonso N et al. beta-(1-->3),(1-->6)-Glucans: medicinal activities, characterization, biosynthesis and new horizons. Appl Microbiol Biotechnol. Oct 2015;99(19):7893-7906.
63. Liu Q et al. Tumor-Educated CD11bhighIalow Regulatory Dendritic Cells Suppress T Cell Response through Arginase I. The Journal of Immunology. May 15, 2009 2009;182(10):6207-6216.
64. Ning Y et al. beta-glucan restores tumor-educated dendritic cell maturation to enhance antitumor immune responses. International journal of cancer. Journal international du cancer. Jun 1 2016;138(11):2713-2723.
65. Perez-Martinez A et al. Arabinoxylan rice bran (MGN-3/Biobran) enhances natural killer cell-mediated cytotoxicity against neuroblastoma in vitro and in vivo. Cytotherapy. May 2015;17(5):601-612.
66. Cholujova D et al. MGN-3 arabinoxylan rice bran modulates innate immunity in multiple myeloma patients. Cancer immunology, immunotherapy: CII. Mar 2013;62(3):437-445.
67. Weiskopf D et al. The aging of the immune system. Transpl Int. Nov 2009;22(11):1041-1050.
68. Choi JY et al. Dietary supplementation with rice bran fermented with Lentinus edodes increases interferon-gamma activity without causing adverse effects: a randomized, double-blind, placebo-controlled, parallel-group study. Nutrition journal. 2014;13:35.
69. Maeda H et al. Oral administration of hydrolyzed rice bran prevents the common cold syndrome in the elderly based on its immunomodulatory action. BioFactors (Oxford, England). 2004;21(1-4):185-187.
70. Kim HY et al. A polysaccharide extracted from rice bran fermented with Lentinus edodes enhances natural killer cell activity and exhibits anticancer effects. Journal of medicinal food. Mar 2007;10(1):25-31.
71. Ghoneum M et al. Modified arabinoxylan from rice bran, MGN-3/biobran, sensitizes metastatic breast cancer cells to paclitaxel in vitro. Anticancer research. Jan 2014;34(1):81-87.
72. Ghoneum M et al. Arabinoxylan rice bran (MGN-3/Biobran) provides protection against whole-body gamma-irradiation in mice via restoration of hematopoietic tissues. Journal of radiation research. May 2013;54(3):419-429.
73. Cholujova D et al. BioBran-augmented maturation of human monocyte-derived dendritic cells. Neoplasma. 2009;56(2):89-95.
74. Ghoneum M et al. Synergistic apoptotic effect of arabinoxylan rice bran (MGN-3/Biobran) and curcumin (turmeric) on human multiple myeloma cell line U266 in vitro. Neoplasma. 2011;58(2):118-123.
75. Ghoneum M et al. Augmentation of macrophage phagocytosis by modified arabinoxylan rice bran (MGN-3/biobran). International journal of immunopathology and pharmacology. Sep-Dec 2004;17(3):283-292.
76. Ghoneum M et al. Mgn-3/biobran enhances generation of cytotoxic CD8+ T cells via upregulation of dec-205 expression on dendritic cells. International journal of immunopathology and pharmacology. Oct-Dec 2014;27(4):523-530.
77. Sheeja K et al. Andrographis paniculata downregulates proinflammatory cytokine production and augments cell mediated immune response in metastatic tumor-bearing mice. Asian Pacific journal of cancer prevention: APJCP. 2010;11(3):723-729.
78. Ji LL et al. Andrograpanin, a compound isolated from anti-inflammatory traditional Chinese medicine Andrographis paniculata, enhances chemokine SDF-1alpha-induced leukocytes chemotaxis. Journal of cellular biochemistry. Aug 1 2005;95(5):970-978.
79. Goronzy JJ et al. Understanding immunosenescence to improve responses to vaccines. Nat Immunol. 2013;14(5):428-436.
80. Grubeck-Loebenstein B et al. Immunosenescence and vaccine failure in the elderly. Aging Clin Exp Res. Jun 2009;21(3):201-209.
81. McElhaney JE et al. The unmet need in the elderly: how immunosenescence, CMV infection, co-morbidities and frailty are a challenge for the development of more effective influenza vaccines. Vaccine. Mar 9 2012;30(12):2060-2067.
82. Xu Y et al. Modulation of immune response in mice immunised with an inactivated Salmonella vaccine and gavaged with Andrographis paniculata extract or andrographolide. International immunopharmacology. Apr 2007;7(4):515-523.
83. Ebrahimi M et al. Purified Protein Fraction of Garlic Extract Modulates Cellular Immune Response against Breast Transplanted Tumors in BALB/c Mice Model. Cell journal. Spring 2013;15(1):65-75.
84. Purev U et al. Individual differences on immunostimulatory activity of raw and black garlic extract in human primary immune cells. Immunopharmacology and immunotoxicology. Aug 2012;34(4):651-660.
85. Kyo E et al. Immunomodulatory effects of aged garlic extract. The Journal of nutrition. Mar 2001;131(3s):1075s-1079s.
86. Ried K. Garlic Lowers Blood Pressure in Hypertensive Individuals, Regulates Serum Cholesterol, and Stimulates Immunity: An Updated Meta-analysis and Review. The Journal of nutrition. Feb 2016;146(2):389s-396s.
87. Percival SS. Aged Garlic Extract Modifies Human Immunity. The Journal of nutrition. Feb 2016;146(2):433s-436s.
88. Ghazanfari T et al. Garlic induces a shift in cytokine pattern in Leishmania major-infected BALB/c mice. Scandinavian journal of immunology. Nov 2000;52(5):491-495.
89. Kyo E et al. Prevention of psychological stress-induced immune suppression by aged garlic extract. Phytomedicine: international journal of phytotherapy and phytopharmacology. Nov 1999;6(5):325-330.
90. Jin JO et al. Fucoidan can function as an adjuvant in vivo to enhance dendritic cell maturation and function and promote antigen-specific T cell immune responses. PloS one. 2014;9(6):e99396.
91. Negishi H et al. Supplementation of elderly Japanese men and women with fucoidan from seaweed increases immune responses to seasonal influenza vaccination. The Journal of nutrition. Nov 2013;143(11):1794-1798.
92. Lee JH et al. The sulfated polysaccharide fucoidan rescues senescence of endothelial colony-forming cells for ischemic repair. Stem cells (Dayton, Ohio). Jun 2015;33(6):1939-1951.
93. Aranha I et al. Immunostimulatory properties of the major protein from the stem of the Ayurvedic medicinal herb, guduchi (Tinospora cordifolia). Journal of ethnopharmacology. Jan 31 2012;139(2):366-372.
94. Bala M et al. Validation of ethnomedicinal potential of Tinospora cordifolia for anticancer and immunomodulatory activities and quantification of bioactive molecules by HPTLC. Journal of ethnopharmacology. Dec 4 2015;175:131-137.
95. Bala M et al. Chemical prospection of important ayurvedic plant Tinospora cordifolia by UPLC-DAD-ESI-QTOF-MS/MS and NMR. Natural product communications.Jan 2015;10(1):43-48.
96. Nair PK et al. Immune stimulating properties of a novel polysaccharide from the medicinal plant Tinospora cordifolia. International immunopharmacology. Dec 15 2004;4(13):1645-1659.
97. Pandey VK et al. G1-4A, a polysaccharide from Tinospora cordifolia induces peroxynitrite dependent killer dendritic cell (KDC) activity against tumor cells. International immunopharmacology. Dec 2014;23(2):480-488.
98. Rege N et al. Immunotherapy with Tinospora cordifolia: a new lead in the management of obstructive jaundice. Indian journal of gastroenterology: official journal of the Indian Society of Gastroenterology. Jan 1993;12(1):5-8.
99. Sannegowda KM et al. Tinospora cordifolia inhibits autoimmune arthritis by regulating key immune mediators of inflammation and bone damage. International journal of immunopathology and pharmacology. Dec 2015;28(4):521-531.
参考来源:
美国医学图书馆
www.nlm.nih.gov
维基百科-免疫衰老
https://en.wikipedia.org/wiki/Immunosenescence
《美国科学院院报》
www.pnas.org
美国国立公众健康网
https://medlineplus.gov
免责声明和安全信息
- 本信息(包括任何附带资料)不是为了取代医生或有关合格从业人士的建议或忠告。
- 任何人如果想要对本文涉及的药物、饮食、运动或其他生活方式的使用、或改变调整,以预防或治疗某一特定健康状况或疾病,应首先咨询医生或有关合格从业人士,并获得他/她们的许可。妊娠和哺乳妇女在使用本网站任何内容前,尤其应征求医生的意见。
- 除非另有说明,本网站所述内容仅适用于成人。
- 本网站所推荐的任何产品,消费者应该以实际的产品标签内容为准,尤其应关注重要的安全信息以及产品最新信息,包括剂量、使用方法和禁忌症等。
- 由于循证医学研究、文献及有关产品处于不断的变化中,本网站工作人员将尽力更新。
- 本网站不能保证所载文章内容、综合干预方案以及相关成分或产品述及的健康益处,也不承担任何责任。

